快科技11月25日消息,荣耀手机宣布,虞书欣、杨洋成为荣耀300系列全球代言人。...
- 首页 比PROTAC应用更广泛的溶酶体降解技术的发展和挑战
比PROTAC应用更广泛的溶酶体降解技术的发展和挑战
靶向蛋白质降解技术是近十年来迅速发展起来的一项干扰蛋白质功能的重要技术,目前研究最多的是基于泛素化-蛋白酶体系统(UPS)的蛋白水解靶向嵌合体(PROTAC)和分子胶技术。然而随着降解机制和降解对象的拓展,近几年相继涌现出各类新型靶向蛋白质降解技术,包括溶酶体靶向嵌合体(lysosome-targeting chimera, LYTAC)技术、自噬靶向嵌合体(autophagytargeting chimera, AUTAC)技术、自噬小体绑定化合物(autophagosome-tethering compound, ATTEC)技术以及分子伴侣介导的自噬(chaperone-mediated autophagy, CMA)嵌合体技术。新兴的靶向蛋白质降解技术探索真核细胞内的另一重要蛋白质降解体系——溶酶体降解系统,如内吞-溶酶体途径和自噬-溶酶体途径[1]。从目前靶向溶酶体降解的技术来看,溶酶体降解途径拥有比UPS更大的使用广度,包括不限于蛋白质、蛋白质多聚体、细胞器等,而且范围不限于胞内或胞外。在此前的文章中,我们曾对溶酶体降解途径进行综述,并与UPS做了区分对比。本次,我们将对溶酶体降解技术的最新进展及优缺点进行分析,以期带来更多的思考。
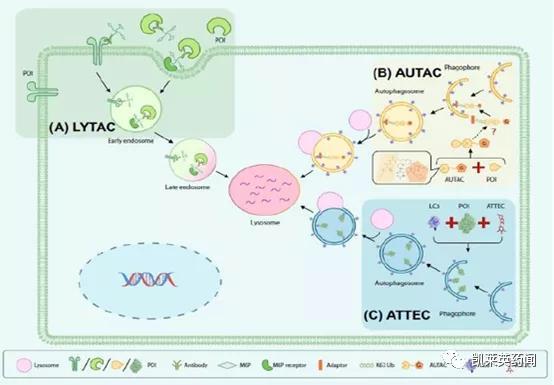
图片来源:分析测试百科
一 基于内吞-溶酶体途径:LYTAC
LYTAC主要由两个结合域组成,其中一个是靶向细胞表面的溶酶体靶向受体(LTR)的寡聚糖结构,另外一个是靶向靶蛋白的抗体、多肽或小分子,两者通过一个化学链连接在一起。LYTAC的作用机制包括:首先,靶蛋白配体部分与靶蛋白的胞外结构域结合,同时寡糖结构与细胞表面的LTR结合,三者形成LTR-LYTAC-靶蛋白三元复合物;随后,复合物经网格蛋白介导内吞进入细胞内,并经囊泡运送到早期内体中;随着内体酸化,三元复合物中的LTR解离并回到细胞膜或高尔基体,LYTAC与靶蛋白的复合物被继续转运至溶酶体中降解 [2]。目前已报道的LTR有两种,分别是非阳离子依赖型甘露糖-6-磷酸受体(CI-M6PR)和去唾液酸糖蛋白受体(ASGPR);其对应的配体分别是多聚甘露糖-6-磷酸(M6P)和N-乙酰半乳糖胺(GalNAc)。2021年3月,Bertozzi课题组[3]设计出一种三联GalNAc分子(tri-GalNAc),通过“点击”化学偶联到能特异性识别靶蛋白的抗体结构上,得到具有肝细胞特异性的GalNAc-LYTAC;此外,该课题组将LYTAC的靶蛋白配体进行简化,将tri-GalAc与靶向细胞整合素的多肽分子进行偶联,设计出的多肽类的LYTAC分子,可选择性地降解肝癌细胞表面的整合素,进而抑制肝癌细胞增殖。同时,Tang课题组[4]也报道了关于GalNAc-LYTAC的研究,该课题组通过将tri-GalNAc与生物素、抗体或抗体片段偶联合成LYTAC分子,成功降解了肝脏细胞的胞外蛋白鼠抗兔IgG-647、鼠抗生物素IgG-647与膜蛋白EGFR。
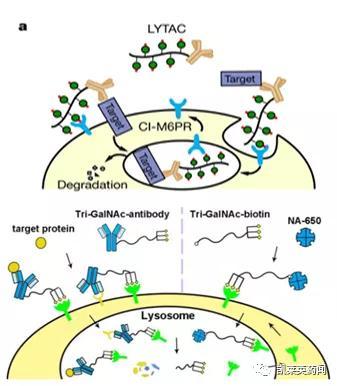
图片来源:文献[2-3]
目前LYTAC技术存在一些问题和挑战,其中包括:①两种LYTAC结构中糖结构与抗体的偶联方式均为非特异性,糖结构与靶蛋白配体的最优化学计量比和两者的最佳连接位点仍无法确定。②研究表明,非特异性糖基修饰的抗体在小鼠体内会被很快清除,如何调节LYTAC的药代动力学特性以控制LYTAC的脱靶清除率,是该技术面临的另一难点。③LYTACs分子的LTR配体是化学合成的非天然糖结构,在人体内可能产生较强免疫原性。④LTR在大多数细胞表面广泛表达,避免LYTAC分子靶向只表达LTR但不表达靶蛋白的细胞,以及提高LYTACs的选择性与安全性,也是亟待解决的问题。⑤目前已被报道的LYTAC主要是抗体类大分子,小分子类LYTAC仍有待开发。
二 基于自噬-溶酶体途径
01 AUTAC
2019年Arimoto课题组[5]首次提出AUTAC的概念。AUTAC的作用原理是通过降解标签模拟S-鸟苷酸化修饰,诱导靶蛋白的多聚泛素化,进而招募自噬体实现溶酶体途径降解。该课题组通过将鸟苷酸衍生物(FBnG)与靶蛋白结合部分连接,有效实现多种疾病相关的靶蛋白的降解,包括甲硫氨酸氨基肽酶2(MetAP2)、FK506结合蛋白(FKBP12)、BET家族蛋白,并开展相关实验证明AUTAC分子是通过自噬-溶酶体途径实现蛋白质的降解;此外,他们还设计靶向线粒体转运蛋白配体TSPO的AUTAC分子,成功实现碎片化线粒体的降解。
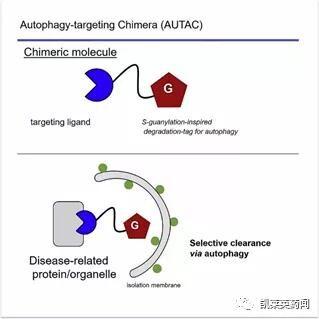
图片来源:文献[5]
AUTAC需要解决的问题包括:①AUTAC的潜能还需要进一步开发,包括探究AUTAC是否可以降解蛋白聚集体;②具体降解机制仍尚未清楚,对AUTAC的多聚泛素化降解标签如何发挥作用仍需进一步研究[6];③AUTAC降解速度比PROTACs慢,一般PROTAC降解过程只需要约1 h,而AUTAC降解需要几个小时。
02 ATTEC
2019年复旦大学的Ding等[7]首次报道利用ATTEC启动自噬途径,降解细胞内聚集的HTT突变蛋白。该课题组通过高通量筛选,从一个由3375个小分子组成的化合物库中筛选出候选ATTEC小分子,并对其进行结构优化,使其能特异性地结合LC3或HTT突变蛋白,但不能与野生型HTT蛋白结合。研究者在细胞水平上证明优化后的ATTEC分子通过直接与HTT突变蛋白和LC3结合,促进HTT突变蛋白被自噬体吞噬,并在动物模型上对ATTEC的疗效进行验证。
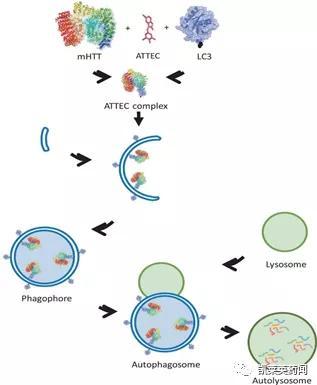
图片来源:文献[8]
总结来说,ATTEC技术具有以下几点优势:①相比于PROTAC技术,ATTEC不需要泛素化途径介导降解,因此不存在蛋白酶体不充足、靶向E3连接酶导致耐药性等难题[8];②ATTEC分子不需要连接子的介入,分子量较低,穿膜活性好,能够更好地满足药代动力学等要求,因此可能具有更好的药物特性。但是,ATTEC还有以下需解决的问题:①分子设计成本比较高,如何高效地设计出能够靶向LC3等自噬相关蛋白的化合物,是亟待解决的一个问题;②ATTEC分子的作用是否会影响整体自噬活性,如何避免自噬相关蛋白和细胞器的非特异性降解,仍有待进一步探究。
03 靶向CMA的嵌合体
CMA的作用机制如下:首先,分子伴侣热休克蛋白HSP70的复合物识别靶蛋白的KFERQ 基序,与靶蛋白形成大复合物;随后,该大复合物与溶酶体相关膜蛋白2A(LAMP2A)相互作用[9],导致LAMP2A低聚化,进而介导靶蛋白与Hsc70复合物进入溶酶体,从而实现降解。2014年Wang课题组[10]利用CMA途径设计出一种嵌合多肽,用于诱导分子伴侣介导的自噬。该课题组设计了由死亡相关蛋白激酶1(DAPK1)结合区域、CMA靶向基序(CTM)和穿膜肽TAT47-57组成的多肽,证明其能够通过溶酶体靶向降解cDAPK1。此外,该设计除了实现cDAPK1的降解外,还成功应用到α-突触核蛋白(α-synuclein)和后突触密度蛋白95(PSD-95)的靶向降解。Xu课题组[11]在研究亨廷顿互作蛋白1相关蛋白(HIP1R)诱导PD-L1降解机制的研究中,发现HIP1R上的多肽基序(MDFSGLSLIKLKKQ)具有与KFERQ基序类似的溶酶体靶向活性,可应用于溶酶体靶向的蛋白质降解。利用HIP1R的结构功能特征,该课题组设计了PDLYSO多肽,该多肽含有PD-L1结合的多肽基序以及溶酶体靶向的多肽基序,可实现PD-L1在溶酶体的降解。Zhou等[12]设计了由细胞周期蛋白依赖性激酶5(CDK5)的配体、穿膜肽Tat和CMA靶向基序CTM组成的Tat-CDK5配体-CTM嵌合多肽,该多肽能够阻断CDK5与受体的结合,最终介导CDK5的溶酶体降解。
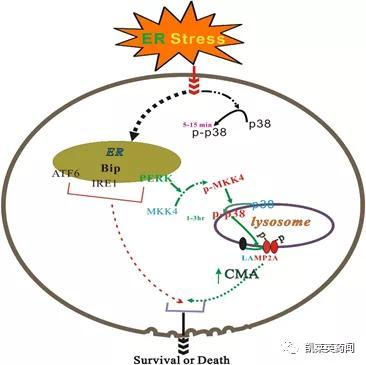
图片来源:文献[9]
靶向CMA的嵌合体技术相比于RNA干扰降解蛋白等技术,具有更快的降解速度、更优的可逆性和剂量依赖性、更强的专一性等优点。另外,相比于靶向降解蛋白的小分子化合物,肽段可能更容易设计,合理利用噬菌体筛选、肽阵列、计算机随机模拟设计等来筛选目标蛋白结合区域,可更高效地获得高选择性和高亲和力的肽段[13]。但是,这项技术也具有一定的局限性和挑战:①通过靶向CMA来实现自噬体途径的降解需要所设计的嵌合多肽与靶蛋白具有较高的亲和性;②嵌合多肽存在的跨膜能力差和稳定性低等问题是影响其最终成药的主要障碍。
三 重点企业及技术情况
01 LYTAC
专注于LYTAC开发的Lycia Therapeutics是一家成立于2019年的生物技术公司,通过自身的LYTAC平台来发现和开发一流的疗法,降解驱动一系列难以治疗疾病包括癌症和自身免疫性疾病的胞外和跨膜蛋白。2021年8月,礼来宣布与Lycia达成合作,利用Lycia的LYTAC蛋白质降解技术发现、开发和商业化新型靶向疗法。2021年9月,Lycia宣布完成7000万美元的B轮融资。目前针对LYTAC的开发成果主要第一代的M6Pn-LYTAC和第二代的GalNAc-LYTAC。第一代LYTAC成功实现了对载脂蛋白E4、EGFR、CD71和PD-1的降解,证明了LYTAC平台的适用性;第二代LYTAC在第一代的基础上进一步探索了其他溶酶体靶向受体的可能性,通过将 ASGPR 的配体和EGFR的抗体ctx偶联,成功实现了肝细胞特异性的EGFR的降解,且不会造成肝脏细胞毒性。
事实上,制药巨头中,除了礼来,诺华也已布局了类似LYTAC的技术。根据已公开的专利(WO2021156792)显示,诺华开发的双功能化合物也是通过溶酶体降解降低细胞外目标分子的血浆水平,这种双功能分子由“一个细胞表面受体配体”连接“一个能结合细胞外靶分子的配体”组成。其中细胞表面受体(包括ASGPR和M6PR)与内吞作用相关,与LYTAC非常类似。
02 ATTEC
在ATTEC领域,PAQ Therapeutics(济景医药)在今年7月宣布完成3000万美元A轮融资,由夏尔巴投资领投,华盖资本、和玉资本、Merck Research Lab、风险基金、巢生基金、经纬中国跟投。PAQ独创的ATTEC技术平台,将扩展自噬作用的治疗潜力,不但可以靶向降解导致疾病的蛋白,还可以通过降解脂类、病原体或其它目标底物来恢复健康,目前的适应症聚焦于神经退行性疾病。2021年8月,发表于Cell Research杂志上的一篇论文中已经证实[14] ATTEC技术还能够降解细胞内储存脂肪的一种细胞器——脂滴(脂滴的过分储积可能与多种疾病相关,比如肥胖、非酒精性脂肪肝、神经退行性疾病等),实现了靶向降解技术从蛋白向非蛋白物质的突破。

03 ATTEC
CreativeBiolabs专注于开发具有所需特异性和亲和力的新型抗体或等效物,其中包括ATTEC设计和筛选,以及ATTEC的体外/体内评估,并在亨廷顿病 (HD)中进行了测试。HD是一种神经退行性疾病,由具有扩展的聚谷氨酰胺 (polyQ) 拉伸的突变 HTT (mHTT) 蛋白引起。这些与mHTT和LC3相互作用的接头化合物可以将分子束缚在一起,以增强mHTT向自噬体的募集,促进其降解;此外,不与野生型 HTT (wtHTT)相互作用的mHTT-LC3接头化合物可能会促进mHTT的等位基因选择性降解。
04 CMA
Life Biosciences是一家针对衰老生物学的先驱生命科学公司,2021年4月发表其临床前研究[15],证明其伴侣介导的自噬激活剂平台在阿尔茨海默病小鼠模型中的临床益处。这项研究表明,即使在出现神经功能障碍之后,在两种不同的阿尔茨海默病小鼠模型中,使用Life Biosciences的一种工具口服化合物上调CMA也能显着改善神经功能并减少不溶性蛋白质聚集体的积累。

展望
LYTAC技术通过靶向内吞-溶酶体途径,降解胞外蛋白和膜蛋白;此外,CMA嵌合体、AUTAC和ATTEC等通过靶向自噬途径的蛋白质降解技术,能够降解错误折叠蛋白、蛋白多聚体或受损细胞器,未来有希望在神经退行性疾病和代谢性疾病的治疗上得以应用。尽管每种技术都有其优点和缺点,新兴的降解技术还处于初级发展阶段。期待溶酶体降解技术能够像PROTAC一样,早日进入临床开发阶段,如果真能实现胞外、膜结合、胞内蛋白灵活降解,或将带来医学领域的颠覆性突破。
[1] 刘京虹,陈怡敏,蔡晓青.靶向蛋白质降解的新兴技术及其研究进展[J/OL].药学学报:1-17
[2] Banik S M, Pedram K, Wisnovsky S, et al. Lysosome-targeting chimaerasfor degradation of extracellular proteins[J]. Nature, 2020, 584(7820): 291-297.
[3] Ahn G, Banik S M, Miller C L, et al. LYTACs that engage theasialoglycoprotein receptor for targeted protein degradation[J]. NatureChemical Biology, 2021: 1-10.
[4] Zhou Y, Teng P, Montgomery N T, et al. Development of triantennaryN-acetylgalactosamine conjugates as degraders for extracellular proteins[J].ACS central science, 2021, 7(3): 499-506.
[5] Takahashi D, Moriyama J, Nakamura T, et al. AUTACs: cargo-specificdegraders using selective autophagy[J]. Molecular cell, 2019, 76(5): 797-810.e10.
[6] Takahashi D, Arimoto H. Targeting selective autophagy by AUTACdegraders[J]. Autophagy, 2020, 16(4): 765-766.
[7] Li Z, Wang C, Wang Z, et al. Allele-selective lowering of mutant HTTprotein by HTT–LC3 linker compounds[J]. Nature, 2019, 575(7781): 203-209.
[8] Li Z, Zhu C, Ding Y, et al. ATTEC: a potential new approach to targetproteinopathies[J]. Autophagy, 2020, 16(1): 185-187.
[9] Li W, Nie T, Xu H, et al. Chaperone-mediated autophagy: Advances frombench to bedside[J]. Neurobiology of disease, 2019, 122: 41-48.
[10] Fan X, Jin WY, Lu J, et al. Rapid andreversible knockdown of endogenous proteins by peptide-directed lysosomaldegradation [J]. Nat Neurosci, 2014, 17: 471-480.
[11] Wang H, Yao H, Li C, et al. HIP1R targetsPD-L1 to lysosomal degradation to alter T cell–mediated cytotoxicity [J]. NatChem Biol, 2019, 15: 42-50.
[12] Zhou YF, Wang J, Deng MF, et al. The peptide-directedlysosomal degradation of CDK5 exerts therapeutic effects against stroke [J].Aging Dis, 2019, 10: 1140-1145.
[13] Mason JM. Design and development of peptidesand peptide mimetics as antagonists for therapeutic intervention [J]. FutureMed Chem, 2010, 2: 1813-1822.
[14] De Vita E, Lucy D, Tate E W. Beyond targeted protein degradation: LD·ATTECs clear cellular lipid droplets[J]. Cell Research, 2021, 31(9): 945-946.
[15] Bourdenx M, Martín-Segura A, Scrivo A, et al. Chaperone-mediatedautophagy prevents collapse of the neuronal metastable proteome[J]. Cell, 2021,184(10): 2696-2714. e25
本文转载自其他网站,不代表健康界观点和立场。如有内容和图片的著作权异议,请及时联系我们(邮箱:guikequan@hmkx.cn)
来源:健康界
北美美国华人导航网 提供最新的华人资讯及最便利的网站提交 请多关注小彩圈网
同类新闻


11月25日消息,据外媒报道称,日本农林水产省11月公布的最新数据,10月份日本...

据分析师声称,目前已经得到了供应链方面的证实,苹果iPhoneSE4将如预期中的...

临海筑梦,阔步扬帆,国之重器,始于创新。我们用试错探索创新之路上的未知挑战,也同...

有人认为,科技与艺术是完全不相干的领域,颇有点“鸡犬相闻,老死不相往来”的架势。...

一台手机、一个人直播、一个人递产品,在上海举办的第五届长三角文博会上,贵州展馆内...